一、引言
β-地中海贫血(β-Thalassämie)与镰状细胞病(Sickle Cell Disease,SCD)是两种由基因突变引起的严重遗传性血液疾病,患者终生面临贫血、输血依赖、血管阻塞危象及多器官损害等挑战。长期输血虽能维持生命,但会带来铁过载等并发症。传统治疗方式主要依赖造血干细胞移植,但受限于合适供体的缺乏。
2024年,基于CRISPR-Cas9基因编辑技术的细胞治疗药物 Casgevy(Exagamglogene Autotemcel) 获得欧洲药品管理局(EMA)的批准,成为首个以基因编辑方式治疗这两种血液疾病的创新疗法。该疗法在2024年被《时代》杂志评为“年度200项最佳发明”之一,2025年1月正式获EMA全面批准,标志着精准医学与基因治疗进入新的里程碑。
二、适应症
Casgevy适用于12岁及以上、符合以下条件的患者:
输血依赖性β-地中海贫血(TDT)患者;
严重镰状细胞病(SCD)患者,且伴有反复发作的血管阻塞危象(VOC);
同时无合适造血干细胞供者可供移植。
这意味着Casgevy为无法接受传统移植的患者提供了新的、潜在治愈性的治疗选择。
三、治疗原理
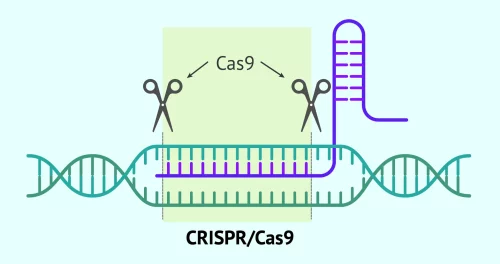
Casgevy是一种自体造血干细胞基因编辑疗法,利用CRISPR-Cas9技术对患者自身的造血干细胞进行精确的基因修饰。
具体机制如下:
在患者造血干细胞中,通过CRISPR技术关闭BCL11A基因的调控作用;这一改变促使细胞重新表达胎儿型血红蛋白(HbF);HbF能有效替代缺陷的成人型血红蛋白,从根本上改善贫血并减少红细胞变形与血管阻塞。
因此,Casgevy不是对症治疗,而是直接针对致病机制的根源进行修复。
四、用法与剂量
Casgevy的治疗过程复杂且个体化,包括以下步骤:
采集阶段:通过单采术(Apherese)收集患者的造血干细胞(CD34+细胞);
基因编辑阶段:在实验室中对这些干细胞进行CRISPR编辑,修复BCL11A调控区;
患者预处理:在细胞回输前,患者需接受髓系清除性预处理化疗(myeloablative conditioning),以清空骨髓,为新细胞“腾位”;
回输阶段:将编辑后的细胞以一次性静脉输注形式回输体内。
推荐剂量为3×10⁶个CD34+细胞/kg体重。
五、禁忌与注意事项
下列情况禁止使用Casgevy:
对药物活性成分或辅料过敏者;
曾接受过异基因或自体造血干细胞移植者;
存在活动性HIV、HBV或HCV感染者。
治疗前需进行严格的感染筛查与全身评估。
六、药物相互作用
为避免药物间干扰,治疗前后需调整或暂停部分药物:
铁螯合剂:治疗前7天及治疗后6个月内停用;
羟基脲、Voxelotor、Crizanlizumab:治疗前至少8周停用;
骨髓抑制性药物:治疗前至少3个月停用。
七、临床研究与疗效
Casgevy的疗效来源于两项开放性、多中心、单臂临床研究,以及一项长期随访研究。
1. β-地中海贫血研究
共有59名患者入组,54名接受Casgevy治疗。
主要终点: 连续12个月无需输血(TI12)。
结果:
42名患者(92.9%)实现了TI12;
所有实现TI12的患者血红蛋白(Hb)及胎儿血红蛋白(HbF)水平均显著上升;
中位输血独立持续时间为22.3个月。
2. 镰状细胞病研究
入组患者均在研究前一年内经历至少2次血管阻塞危象(VOC)。
结果:
93.5%的患者在治疗后12个月内无VOC发作;
未出现与Casgevy直接相关的严重安全事件。
3. 长期随访
正在进行的长期随访研究表明,Casgevy的疗效持久且安全性稳定,未发现新的安全隐患。
八、妊娠与哺乳
Casgevy在妊娠期间禁用,因可能对胚胎具有毒性或致畸性。
哺乳期患者应在治疗前停止哺乳。
目前尚无关于生育能力影响的充分数据。
九、总结与展望
Casgevy的批准是基因治疗领域的重大突破。作为全球首个获批的CRISPR基因编辑疗法,它不仅为β-地中海贫血和镰状细胞病患者提供了潜在的根治机会,也证明了基因编辑在临床应用中的安全性与可行性。
未来,随着更多长期随访结果的公布,Casgevy有望成为更多遗传性血液疾病的治疗模板,为全球数百万罕见病患者带来新的希望。